公司簡介
泰宗生物科技(4169) 創立於1989年,係具研發、通路、有盈利、營收穩健成長之新藥開發公司。公司總部設於新北汐止區,擁有通過LDTS、ISO17025 認證的分子檢測實驗室、GDP 評鑑核准之藥品醫材倉儲及醫材冷鏈倉儲。泰宗突破了傳統生技公司早期常面臨的高風險與長期虧損,以穩健的通路現金流做為後盾,目前核心研發產品皆已邁入後期收成階段,準備大步邁向國際舞台。
研發與通路並行策略
生技產業的研發需要漫長時間與龐大資金,而泰宗憑藉「營運帶動研發、研發推動成長」的雙軌發展策略,已在資本市場與醫療通路中站穩腳步。在營運端,泰宗目前的營收主體以自有的西藥產品與醫療器材銷售或代理銷售為主。
公司深入全台醫學中心及區域醫院,通路亦觸及地區醫院及專科診所,建立起極度綿密的「醫療通路」網,帶來了穩定且持續成長的現金流,大幅降低新藥研發的資金不確定性。更重要的是,這張深廣的終端醫療通路網,將成為未來泰宗自有研發之新藥與檢測產品上市後,能夠快速進入市場轉換成營收的強力後盾。
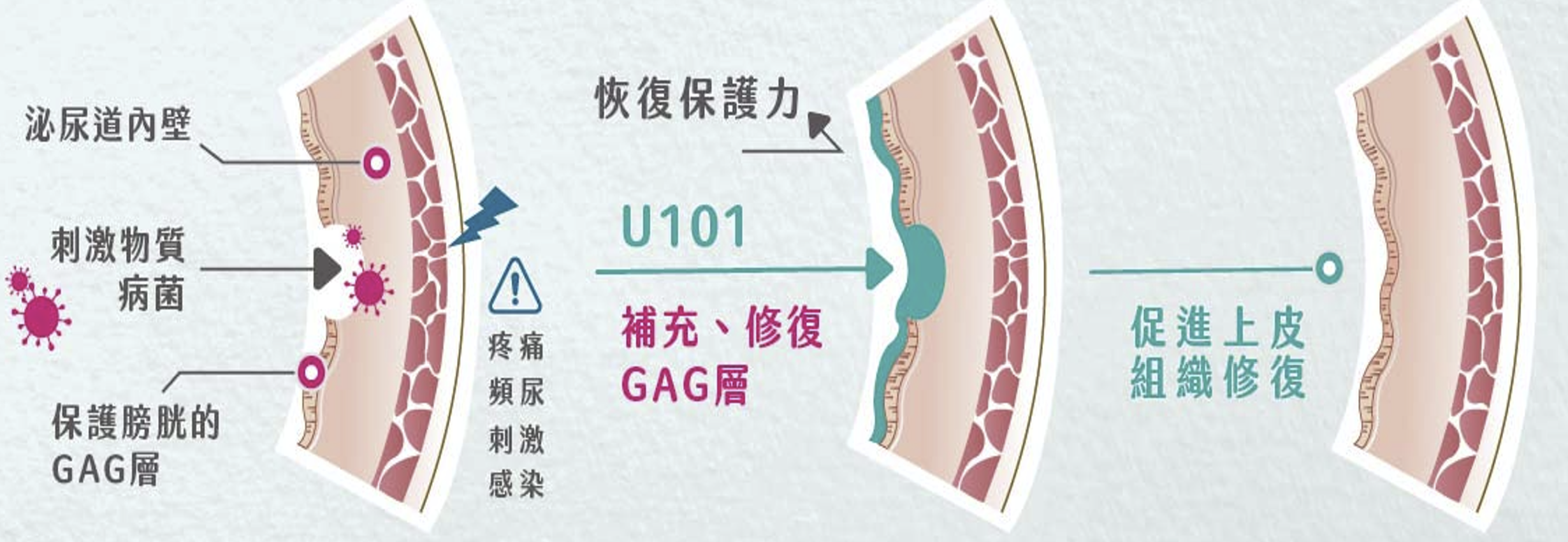
新藥U101:全球首創非抗生素療法,瞄準反覆性泌尿道感染龐大商機
在創新研發方面,泰宗精準鎖定臨床上「未被滿足的需求」。其核心新藥U101,是全球首款針對「反覆性泌尿道感染(rUTI)」預防所開發的非抗生素口服新藥。
臨床上,泌尿道感染復發率極高,長期仰賴低劑量抗生素預防易衍生抗藥性問題,而市面上的保健食品在實證效果上又相當有限。全球rUTI潛在患者近1億人,市場規模龐大。U101採用505(b)(2)途徑開發,有效縮短時程,並同步掌握關鍵原料藥。目前U101在台灣已進入第三期樞紐性臨床試驗,預計後續期中分析結果,有望提交台灣新藥許可證(NDA)申請,並同步啟動美國臨床三期。
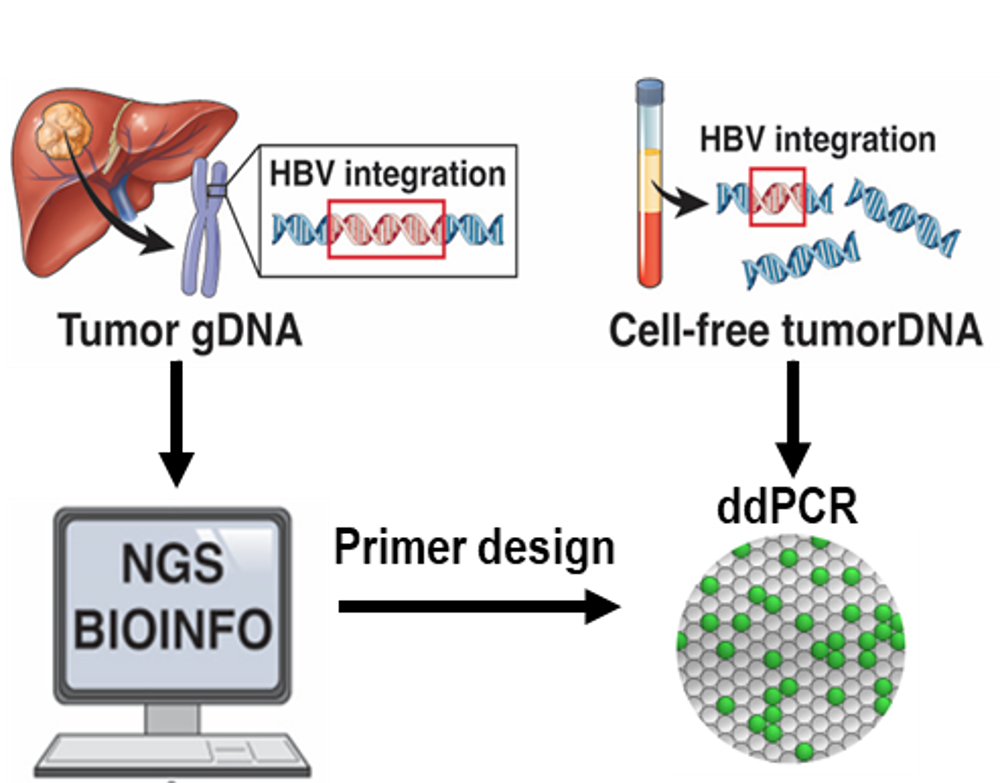
精準醫療 B肝肝癌檢測平台”凱玫樂”:榮獲美 FDA 突破性醫材認定,開創肝癌復發監測新局
針對 B 型肝癌患者術後一年內的復發率高達五成的痛點,泰宗推出了凱玫樂(CatCHimera)肝癌檢測平台。該平台透過血液的液態活檢,結合次世代定序(NGS)與微滴式數位核酸偵測技術(ddPCR),專精於追蹤肝癌特有的 B 肝病毒 DNA 嵌合序列。在靈敏度方面亦優於傳統甲型胎兒蛋白(AFP),尤其在小型腫瘤偵測表現更為突出。此外,其預測復發的陽性預測值(PPV)為71%、陰性預測值(NPV)達92%,平均可較電腦斷層(CT)提早約158天發現復發;若結合AFP與PIVKA-II檢測,靈敏度與特異性更可分別提升至95.8%與95.5%,能比傳統電腦斷層提早3到9個月發現殘存腫瘤細胞。凱玫樂不僅已取得台灣衛福部 LDTS 認證,更獲得美國 FDA 授予「突破性醫材認定」(BDD)。這項殊榮不僅將加速未來在美國的法規審查,更為未來技術授權中國與全球市場打下堅實基礎,鎖定每年 45 萬名新增肝癌病患的龐大追蹤市場。
未來展望
綜觀泰宗生物的企業優勢,穩健的通路銷售確保了公司無畏景氣波動的穩定獲利能力;而U101與凱玫樂兩項邁入臨床後期與取證階段的高潛力產品,則展現了公司的研發能量。